IVDR fordert Aktualisierung der Leistungsbewertung – So schaffen Sie das!
11/10/2022
Do you have any questions about the article or would you like to find out more about our services? We look forward to hearing from you!Make a non-binding enquiry now
Es ist vollbracht: Sie haben die initiale Leistungsbewertung für Ihr Produkt IVDR-konform durchgeführt und in den geforderten Plänen und Berichten dokumentiert. Jetzt können Sie erstmal durchatmen – aber nur bis zur ersten Aktualisierung der Leistungsbewertung Ihres In-vitro-Diagnostikums (IVDs), denn dieses Updating ist Anforderung der IVDR, Art. 56 (6).
Konkret müssen Sie für die Aktualisierung der Leistungsbewertung die Daten nutzen, die sich aus der der Nachbeobachtung nach dem Inverkehrbringen ergeben: Post-Market Surveillance (PMS) und Post Market Performance Follow-Up (PMPF). Das heißt, Sie müssen diese, und wie Ihnen sicher bekannt ist, einige weitere Prozesse zeitlich und inhaltlich aufeinander abstimmen. Nur so stehen Ihnen die benötigten Daten rechtzeitig und aktuell für die Aktualisierung der Leistungsbewertung zur Verfügung.
In diesem Artikel wollen wir Ihnen, den Herstellern, zeigen, wo Gefahren lauern bei der Aktualisierung der Leistungsbewertung. Nutzen Sie unsere Erfahrung und profitieren Sie von unseren Tipps für Ihre Praxis.
Die IVDR nennt nur für Klasse C- und D-Produkte einen konkreten Zeitraum, nämlich „bei Bedarf, mindestens jedoch einmal jährlich“.
Für Klasse A- und B-Produkte hingegen ist kein bestimmter Zeitraum genannt. Aber auch für diese Produkte ist eine Aktualisierung in regelmäßigen Abständen zu planen. Wie groß diese Zeitabstände sind, kommt auf Ihr IVD an:
Achtung! Für alle Risikoklassen gilt: PMS und PMPF können die Aktualisierung der Leistungsbewertung jederzeit triggern! Sobald aus den Daten, die sich aus dem PMS- und PMPF-Prozess ergeben, hervorgeht, dass die Sicherheit und Leistung, und/oder das Nutzen-Risiko-Verhältnis beeinträchtig sind/sein könnten, müssen Sie den klinischen Nachweis entsprechend aktualisieren.Aus dem PMS kann sich z. B. ein neues Risiko ergeben, welches Sie bisher nicht kannten und nicht bewertet haben. Dann müssen Sie eventuell anhand von zusätzlichen Leistungsstudien zeigen, ob und wie die Leistung und das Nutzen-Risiko-Verhältnis des Produkts dadurch beeinträchtigt bzw. nicht beeinträchtigt wird. Oder die Literaturrecherche im Rahmen der PMS hat ergeben, dass es neue Technologien im Fachbereich gibt. Dann müssen Sie ggf. den Stand der Technik (State of the Art) und das Nutzen-Risiko-Verhältnis ihres Produkts überprüfen.
Die nachfolgende Tabelle zeigt die wichtigsten Dokumente und die für die Aktualisierung geforderten Zeiträume: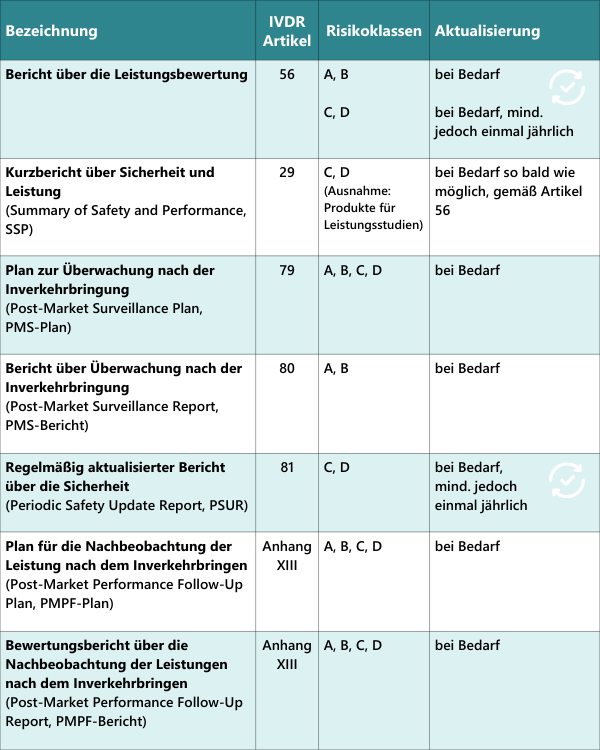
In der Praxis haben wir oft erlebt, dass dieser Punkt nicht leicht umsetzbar ist, da er die effiziente Zusammenarbeit und Abstimmung mehrerer Abteilungen erfordert.
Unsere Empfehlung:Gehen Sie frühzeitig auf die beteiligten Abteilungen zu, um die geforderten Aktivitäten aufeinander abzustimmen. Oftmals ist es einfacher, den Zeitplan der Aktualisierung der Leistungsbewertung an die Zeitplanung des PMS anzupassen als umgekehrt, weil PMS meist schon etabliert ist. Wer das weiß, tut sich leichter.Auch für die inhaltliche Zusammenarbeit ist es mehr als sinnvoll, sich mit den verschiedenen Abteilungen abzusprechen, bzw. deren Prozesse zu kennen, damit Aufgaben nicht doppelt erledigt werden und stattdessen gebündelt abgearbeitet werden können. Oftmals werden im Rahmen von PMS bereits Aktivitäten durchgeführt, die auch für die Aktualisierung der Leistungsbewertung anfallen und somit genutzt werden können, z. B. die Literaturrecherche zum Produkt bzw. zu ähnlichen Produkten oder zum Stand der Technik.Kommen Sie auch hier ins Gespräch, um Redundanzen zu vermeiden. Wenn Sie innerhalb Ihrer PMS-Aktivität schon eine Literaturrecherche zum Produkt durchführen, dann können Sie diese, ggf. nach einigen Anpassungen und inhaltlichen Abstimmungen, auch für Ihre Literaturrecherche zur klinischen Leistung heranziehen. Auch hier sollten Sie darauf achten, dass die Literatursuche zum Zeitpunkt des Abschlusses der Aktualisierung der Leistungsbewertung nicht länger als 6 Monate zurückliegt.
Beispiel: Es wird an einer Stelle der Wortlaut der Zweckbestimmung geändert, jedoch nicht durchgängig in allen Dokumenten der Technischen Dokumentation. Oder die Umsetzung der Produktänderung ist noch nicht abgeschlossen, aber die nächste Aktualisierung steht schon an. In jedem Fall ist es ratsam, die beteiligten Abteilungen an einen Tisch zu bringen, um sich vor geplanten Änderungen abzustimmen.
Angabe der Update-ZyklenDie Erfahrung hat gezeigt, dass gerade anfangs die verschiedenen Prozesse noch nicht wirklich aufeinander eingespielt sind. Vermeiden Sie exakte Datumsangaben bei der Planung Ihres nächsten Updates: Denn es kann immer etwas dazwischenkommen, auch wenn Ihre Planung noch so gut ist. Bewährt hat sich hier die Angabe von Quartalen. So können Sie unvorhergesehene zusätzliche Aufwände meist locker abfangen, ohne Ihre Fristen zum Update zu verletzen.
Beste GrüßeDieser Beitrag stammt ursprünglich von Dr. Anna Rist und Dr. Sandra Reuter. Bei Fragen zum Artikel oder darüber hinaus steht Ihnen Dr. Sandra Reuter jederzeit gerne zur Verfügung.
 Dr. Sandra Reuter
Dr. Sandra Reuter
Konkret müssen Sie für die Aktualisierung der Leistungsbewertung die Daten nutzen, die sich aus der der Nachbeobachtung nach dem Inverkehrbringen ergeben: Post-Market Surveillance (PMS) und Post Market Performance Follow-Up (PMPF). Das heißt, Sie müssen diese, und wie Ihnen sicher bekannt ist, einige weitere Prozesse zeitlich und inhaltlich aufeinander abstimmen. Nur so stehen Ihnen die benötigten Daten rechtzeitig und aktuell für die Aktualisierung der Leistungsbewertung zur Verfügung.
In diesem Artikel wollen wir Ihnen, den Herstellern, zeigen, wo Gefahren lauern bei der Aktualisierung der Leistungsbewertung. Nutzen Sie unsere Erfahrung und profitieren Sie von unseren Tipps für Ihre Praxis.
Wie oft soll die Leistungsbewertung aktualisiert werden?
Wann ein Update der Leistungsbewertung sinnvoll oder gefordert ist, hängt u. a. von der Risikoklasse des betreffenden Produktes ab.Die IVDR nennt nur für Klasse C- und D-Produkte einen konkreten Zeitraum, nämlich „bei Bedarf, mindestens jedoch einmal jährlich“.
Für Klasse A- und B-Produkte hingegen ist kein bestimmter Zeitraum genannt. Aber auch für diese Produkte ist eine Aktualisierung in regelmäßigen Abständen zu planen. Wie groß diese Zeitabstände sind, kommt auf Ihr IVD an:
- Wie sieht die Zweckbestimmung des Produkts aus?
- Welche Risiken gehen vom Produkt aus?
- Wie lange ist das Produkt schon am Markt? Ist es neu, oder hat es sich schon viele Jahre bewährt?
- Wie hoch ist das Tempo des technischen Fortschritts/der neuartigen Entwicklungen im Fachbereich?
Achtung! Für alle Risikoklassen gilt: PMS und PMPF können die Aktualisierung der Leistungsbewertung jederzeit triggern! Sobald aus den Daten, die sich aus dem PMS- und PMPF-Prozess ergeben, hervorgeht, dass die Sicherheit und Leistung, und/oder das Nutzen-Risiko-Verhältnis beeinträchtig sind/sein könnten, müssen Sie den klinischen Nachweis entsprechend aktualisieren.Aus dem PMS kann sich z. B. ein neues Risiko ergeben, welches Sie bisher nicht kannten und nicht bewertet haben. Dann müssen Sie eventuell anhand von zusätzlichen Leistungsstudien zeigen, ob und wie die Leistung und das Nutzen-Risiko-Verhältnis des Produkts dadurch beeinträchtigt bzw. nicht beeinträchtigt wird. Oder die Literaturrecherche im Rahmen der PMS hat ergeben, dass es neue Technologien im Fachbereich gibt. Dann müssen Sie ggf. den Stand der Technik (State of the Art) und das Nutzen-Risiko-Verhältnis ihres Produkts überprüfen.
Welche Dokumente müssen aktualisiert werden?
Die IVDR fordert, dass während des gesamten Lebenszyklus des Produkts die Leistungsbewertung und die dazugehörigen Unterlagen zu aktualisieren sind (s. hierzu auch unsere Grafik IVDR Product Lifecycle Reporting ). Im Fokus steht hierbei der Bericht zur Leistungsbewertung. Aber auch alle anderen Dokumente, die diesen Bericht speisen, wie z. B. der Plan zur Leistungsbewertung, die Berichte zur wissenschaftlichen Validität, analytischen Leistung und klinischen Leistung müssen geprüft und aktualisiert werden.Da sich die Aktualisierung der Leistungsbewertung aus den PMS-Berichten bzw. bei Klasse C und D aus dem Sicherheitsbericht nach Art. 81 (PSUR – Periodic Safety Update Report) und den PMPF-Berichten speist, müssen diese Dokumente ebenfalls regelmäßig und in sinnvollen Zeiträumen aktualisiert werden. Daraus folgen ebenfalls die regelmäßige Überprüfung und Anpassung der zugehörigen Pläne (PMS-Plan, PMPF-Plan).Außerdem muss die Leistungsbewertung eng mit dem Risikomanagement verknüpft werden. Das sollte als kontinuierlicher, iterativer Prozess während des gesamten Lebenszyklus eines Produkts regelmäßig systematisch aktualisiert werden.Die nachfolgende Tabelle zeigt die wichtigsten Dokumente und die für die Aktualisierung geforderten Zeiträume:

Stimmen Sie Ihre Prozesse zeitlich und inhaltlich aufeinander ab!
Sie wissen nun, welche Dokumente von der Aktualisierung der Leistungsbewertung betroffen sind, und dass die Aktualisierung eng mit Post-Market Surveillance (PMS), Post-Market Performance Follow-up (PMPF) und Risikomanagement verzahnt ist. Die entsprechenden Prozesse müssen ineinandergreifen und die Abteilungen sollten unbedingt miteinander kooperieren. Die Aktualisierung der Leistungsbewertung ist aufwändig und Sie sollten, falls Sie es noch nicht getan haben, die Prozesse für die Aktualisierung aufeinander abstimmen und in Ihrem QMS etablieren. Denn was sich in der Theorie logisch darstellt, kann in der Praxis ganz schön herausfordernd sein.Nehmen wir als Beispiel die Abhängigkeit des Updates der Leistungsbewertung von PMS und PMPF. PMS-Bericht bzw. PSUR und PMPF-Bericht sollten bereits vor dem geplanten Update vorliegen. Die Zeitspanne zwischen dem Vorliegen dieser Berichte und dem geplanten Update sollte möglichst kurz gehalten werden, damit die Daten aus den Berichten nicht wieder veraltet sind, wenn das Update abgeschlossen ist. Idealerweise sollte das Update innerhalb eines Quartals abgeschlossen werden, nachdem PSUR/PMS- und PMPF-Berichte vorliegen. Eine Zeitspanne von 6 Monaten sollte nicht überschritten werden.In der Praxis haben wir oft erlebt, dass dieser Punkt nicht leicht umsetzbar ist, da er die effiziente Zusammenarbeit und Abstimmung mehrerer Abteilungen erfordert.
Unsere Empfehlung:Gehen Sie frühzeitig auf die beteiligten Abteilungen zu, um die geforderten Aktivitäten aufeinander abzustimmen. Oftmals ist es einfacher, den Zeitplan der Aktualisierung der Leistungsbewertung an die Zeitplanung des PMS anzupassen als umgekehrt, weil PMS meist schon etabliert ist. Wer das weiß, tut sich leichter.Auch für die inhaltliche Zusammenarbeit ist es mehr als sinnvoll, sich mit den verschiedenen Abteilungen abzusprechen, bzw. deren Prozesse zu kennen, damit Aufgaben nicht doppelt erledigt werden und stattdessen gebündelt abgearbeitet werden können. Oftmals werden im Rahmen von PMS bereits Aktivitäten durchgeführt, die auch für die Aktualisierung der Leistungsbewertung anfallen und somit genutzt werden können, z. B. die Literaturrecherche zum Produkt bzw. zu ähnlichen Produkten oder zum Stand der Technik.Kommen Sie auch hier ins Gespräch, um Redundanzen zu vermeiden. Wenn Sie innerhalb Ihrer PMS-Aktivität schon eine Literaturrecherche zum Produkt durchführen, dann können Sie diese, ggf. nach einigen Anpassungen und inhaltlichen Abstimmungen, auch für Ihre Literaturrecherche zur klinischen Leistung heranziehen. Auch hier sollten Sie darauf achten, dass die Literatursuche zum Zeitpunkt des Abschlusses der Aktualisierung der Leistungsbewertung nicht länger als 6 Monate zurückliegt.
Diese Fallstricke können Sie vermeiden:
Change-ManagementAm Anfang der Aktualisierung der Leistungsbewertung sollte immer auch die Frage nach Produktänderungen seit der letzten Leistungsbewertung stehen. Gab es in der Zwischenzeit einen Design-Change, oder wurde gar die Zweckbestimmung verändert? Wenn ja, wurden die Produktänderungen auch hinsichtlich der Leistung und Sicherheit des Produkts bewertet? Wenn Sie ein gutes und zuverlässiges Change-Management-System implementiert haben und dies auch gelebt wird, sollten solche geplanten Produktänderungen die Aktualisierung der Leistungsbewertung triggern, falls nötig - unabhängig von ihrem geplanten Update-Zyklus.In der Praxis hat sich gezeigt, dass das Änderungsmanagement nicht immer reibungslos funktioniert.Beispiel: Es wird an einer Stelle der Wortlaut der Zweckbestimmung geändert, jedoch nicht durchgängig in allen Dokumenten der Technischen Dokumentation. Oder die Umsetzung der Produktänderung ist noch nicht abgeschlossen, aber die nächste Aktualisierung steht schon an. In jedem Fall ist es ratsam, die beteiligten Abteilungen an einen Tisch zu bringen, um sich vor geplanten Änderungen abzustimmen.
Angabe der Update-ZyklenDie Erfahrung hat gezeigt, dass gerade anfangs die verschiedenen Prozesse noch nicht wirklich aufeinander eingespielt sind. Vermeiden Sie exakte Datumsangaben bei der Planung Ihres nächsten Updates: Denn es kann immer etwas dazwischenkommen, auch wenn Ihre Planung noch so gut ist. Bewährt hat sich hier die Angabe von Quartalen. So können Sie unvorhergesehene zusätzliche Aufwände meist locker abfangen, ohne Ihre Fristen zum Update zu verletzen.
Fazit
Der Zeitaufwand für die Aktualisierung wird häufig unterschätzt. Zwar handelt es sich „nur“ um eine Aktualisierung, aber trotzdem müssen alle Dokumente nochmals angefasst und überprüft werden. Das Einpflegen zusätzlicher neuer Informationen in die Technische Dokumentation ist vielleicht nicht so aufwändig wie die initiale Leistungsbewertung, braucht aber dennoch Zeit und Aufmerksamkeit.An der Beschaffung der Informationen für die Aktualisierung sind in der Regel mehrere Abteilungen beteiligt, die koordiniert zusammenarbeiten müssen, wenn die Aktualisierung effizient und zeitsparend durchgeführt werden soll.Die Aktualisierung der Leistungsbewertung ist also nichts, was man mal eben so nebenbei macht. Sie ist anspruchsvoll, muss gut geplant werden und braucht eigene Prozesse.Wir stehen Ihnen gerne mit Rat und Tat zur Seite, wenn es um die Aktualisierung der Leistungsbewertung Ihrer In-Vitro-Diagnostika geht! Unsere Erstgespräche sind selbstverständlich unverbindlich und kostenfrei – schreiben Sie uns einfach an. Auch wenn Sie Fragen zu anderen Regulatory Affairs-Bereichen haben, ist unser Team für Sie da. Wir freuen uns darauf, Sie kennenzulernen.Beste GrüßeDieser Beitrag stammt ursprünglich von Dr. Anna Rist und Dr. Sandra Reuter. Bei Fragen zum Artikel oder darüber hinaus steht Ihnen Dr. Sandra Reuter jederzeit gerne zur Verfügung.
Our blog posts are researched and created with the utmost care, but are only snapshots of the regulations, which are constantly changing. We do not guarantee that older content is still current or meaningful. If you are not sure whether the article you have read on this page still corresponds to the current state of regulation, please contact us: we will quickly place your topic in the current context.

Team Lead IVD
Regulatory Affairs & Technical Documentation


