Künstliche Intelligenz (KI) und Maschinelles Lernen (ML) halten Einzug in die Welt der In-vitro-Diagnostika (IVD). Damit heben sie den Output von IVD auf ein nächstes Level, konfrontieren die Hersteller aber auch mit neuen regulatorischen Herausforderungen. Denn der europäische AI Act (Verordnung (EU) 2024/1689) gibt erstmals verbindliche Regeln für den Einsatz von KI auch in IVD vor und steigert damit die Anforderungen an die Sicherheit in Diagnostiksystemen.Ja, die regulatorische Last wächst weiter. Doch diese Regulierung hat durchaus ihre Berechtigung und bringt Sie bei erfolgreicher Umsetzung in eine Top-Position: Als Hersteller von IVD mit KI-Anteilen gewinnen Sie neben regulatorischer Sicherheit schließlich auch an Vertrauen im Markt: Sie stellen sicher, dass Ihr IVD mit KI-Anteilen allen Dokumentationspflichten nachkommt, und weisen nach, dass es sicher ist gegenüber Manipulation, Datenverlust und Fehlfunktionen (Stichwort: Cybersecurity), und zwar über den gesamten Lebenszyklus hinweg.Sie planen ein IVD mit KI-Funktion? Verschaffen Sie sich jetzt einen Überblick im unverbindlichen Gespräch mit unseren Expert*innen. Kontaktieren Sie uns!
Unsere Leistungen für Ihr IVD
Zulassungsstrategie entwickeln:
Holen Sie sich mit Metecon die Unterstützung, die Sie brauchen: für die umfassende Analyse der regulatorischen Grundlagen Ihres IVDs mit KI-/ML-Komponente und für die Entwicklung einer passgenauen Zulassungsstrategie, abgestimmt auf geltende europäische und internationale Vorschriften.Anforderungen analysieren und interpretieren:
In Ihrem Auftrag identifizieren und priorisieren wir relevante gesetzliche, normative und regulatorische Anforderungen, darunter den AI Act, die IVDR, ISO/IEC-Normen sowie länderspezifische Richtlinien. Dies könnte sich u. a. beziehen auf: ISO 13485, ISO/IEC 42001, ISO/IEC 23894, ISO 14971, IEC 62304, IEC 81001 5 1, IEC 82304-1 , IEC 60601-1, ISO/IEC 27001, ISO/IEC 27701, IEC TR 80002-1, ISO/IEC 24029, ISO/IEC 23894 und FDA-Guidances.Klarheit durch GAP-Analyse:
Wir decken bestehende Lücken in den Prozessen und im Dokumentationsstand auf und weisen auf fehlende Informationen, Nachweise oder Strukturierungen hin, um regulatorisch vollständig und auditfest zu sein.Die Technische Dokumentation erstellen und optimieren:
Ihre Dokumentation erstellen und ergänzen wir auf Konformität und Prüfbarkeit: von der Leistungsbewertung über das Risikomanagement bis hin zu softwarebezogenen Nachweisen.Prozesse an KI/ML anpassen:
Wir passen Ihre internen Abläufe und QM-Systeme gezielt an, damit KI-spezifische Anforderungen effizient berücksichtigt und dauerhaft implementiert werden können.KI-Datenmanagement installieren:
Gemeinsam etablieren wir ein strukturiertes Datenmanagement, das die Anforderungen an Trainings-, Tuning- und Testdaten durchgängig und lückenlos erfüllt.360°-Begleitung durch Ihre Zulassung:
Wir begleiten Sie umfassend durch den gesamten Zulassungsprozess – von regulatorischen Bewertungen bis zur Auditvorbereitung und -unterstützung.AI Act Mapping & Use-Case-Analyse:
Wie ist Ihr spezifischer Anwendungsfall im Kontext des AI Acts einzuordnen? Welche Artikel und Anforderungen greifen, und welche Maßnahmen ergeben sich daraus? Wir prüfen das für Sie.KI-Systeme absichern und überwachen:
Zusammen mit Ihnen entwickeln wir nachvollziehbare Konzepte für Transparenz, Sicherheit und menschliche Aufsicht von der Architektur bis zur Anwendung.Trainings-, Tuning- & Testdaten bewerten:
Ihre Datenquellen analysieren wir systematisch auf Herkunft, Eignung und regulatorische Anforderungen und helfen damit, die Anforderungen an Nachvollziehbarkeit zu erfüllen.Kommunikation mit Ihrer Benannten Stelle:
Wir bereiten Sie gezielt auf Interaktionen mit Benannten Stellen (EU) oder Behörden (z. B. USA, FDA) vor und stehen bei fachlichen Rückfragen zu KI-spezifischen Themen beratend zur Seite.Workshops & Inhouse-Trainings:
Nutzen Sie unser gezieltes Praxiswissen zur regulatorischen Umsetzung von KI-Systemen, individuell abgestimmt auf den Erfahrungshintergrund und die Aufgaben Ihrer Teams.
Lassen Sie uns gemeinsam prüfen, wie Sie sicher durch die IVDR und den AI Act navigieren. Vereinbaren Sie jetzt Ihr kostenloses Erstgespräch ohne weitere Verpflichtung!
Was bedeutet der AI Act für IVD-Hersteller?
Mit dem AI Act verpflichtet die EU alle Anbieter von KI-Systemen zu umfassenden Transparenz-, Sicherheits- und Dokumentationspflichten. In-vitro-Diagnostika (IVD) mit KI-Anteilen, etwa bei Bildauswertung, Algorithmus-basierter Risikoeinschätzung oder automatisierter Dateninterpretation, gelten nahezu sicher als Hochrisiko-KI-Systeme.Die Einstufung als Hochrisiko-KI-System zieht eine Vielzahl zusätzlicher Pflichten nach sich, wie etwa die Durchführung einer detaillierten Risikoanalyse speziell für die KI-Komponente, die Implementierung technischer und organisatorischer Maßnahmen zur menschlichen Aufsicht, sowie die Pflicht zur Dokumentation von Trainings-, Tuning- und Testdaten. Darüber hinaus muss die gesamte Systemarchitektur so gestaltet sein, dass sie Transparenz, Robustheit und Nachvollziehbarkeit sicherstellt. Diese Anforderungen gelten zusätzlich zur IVDR, nicht stattdessen. Hersteller müssen also zwei komplexe Regelsysteme zugleich bedienen und sorgfältig miteinander verzahnen.Je früher Sie sich mit den Vorgaben auseinandersetzen, desto reibungsloser gelingt die spätere CE-Zulassung. Kommen wir in den Austausch!
Darauf sollten Sie also vorbereitet sein:
- Dokumentation der Trainings-, Test- und Validierungsdaten
- Nachweis von Robustheit, Genauigkeit und Kontrollmechanismen
- transparente Entscheidungsprozesse und erklärbare Systemlogik
- Risikobewertung und Maßnahmen zur Begrenzung unerwünschter Effekte
- Integration der KI-Komponenten in die bestehende IVDR-konforme Dokumentation
Doppelregulierung mit System: MDR/IVDR und AI Act im Zusammenspiel
Der AI Act löst bestehende Regularien wie die IVDR nicht ab; stattdessen ergänzt er sie. Das bringt neue Pflichten mit sich und fordert ein überlegtes Vorgehen, um eine bestmögliche Verzahnung beider Regelwerke sicherzustellen:
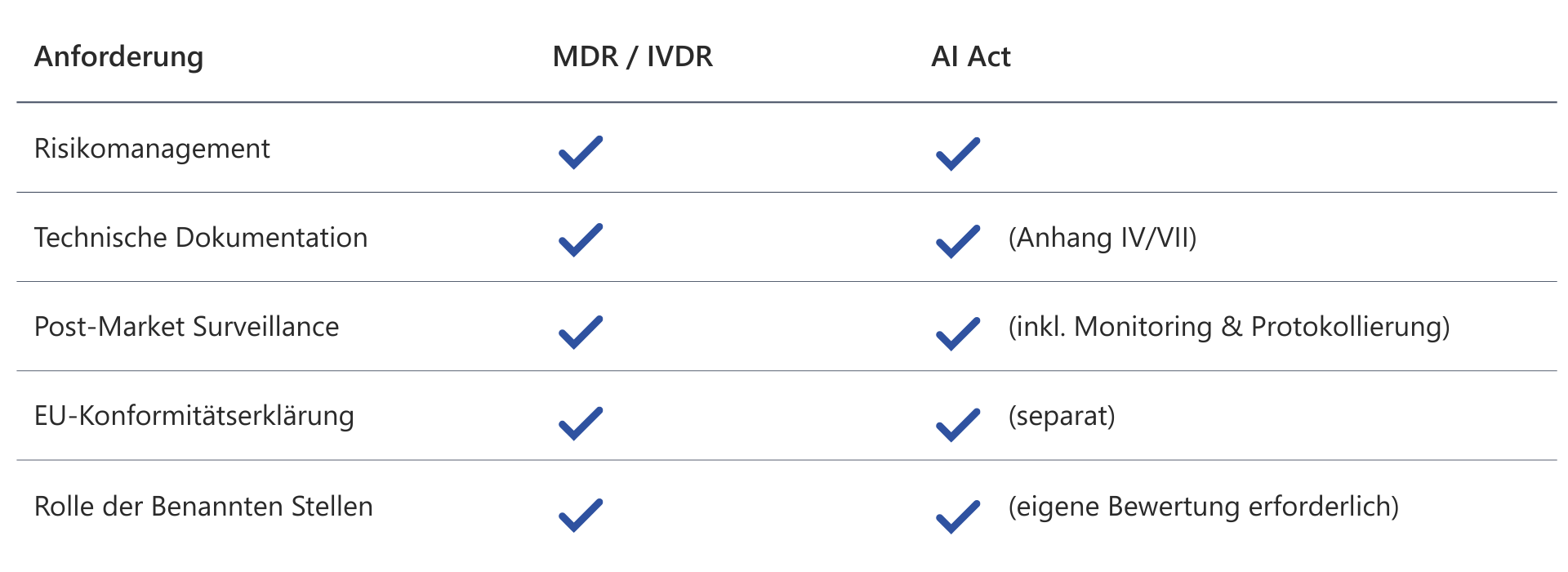
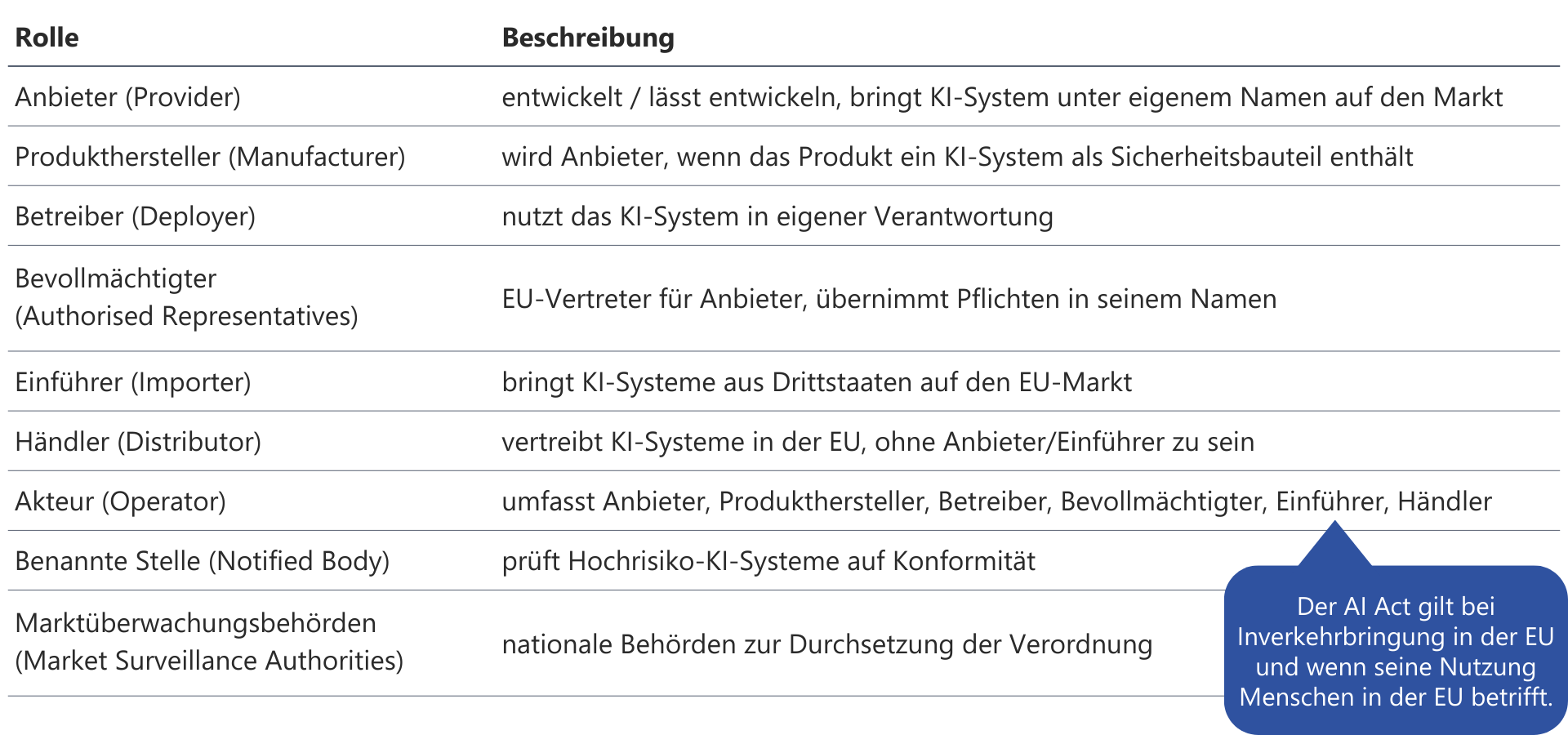
AI Act: Zentrale Begriffe und Konzepte kompakt erklärt
Der AI Act gilt bei Inverkehrbringung in der EU und wenn seine Nutzung Menschen in der EU betrifft.
Übergangsfristen des AI Acts: Was IVD-Hersteller jetzt wissen müssen
Seit Februar 2025 ist der AI Act offiziell in Kraft. Für Hersteller von IVD-Produkten mit KI-Komponenten beginnt damit eine Übergangsphase, in der Weichenstellungen entscheidend sind. Denn ab 2027 werden die neuen Anforderungen verbindlich kontrolliert.Unsere Empfehlung: Prüfen Sie frühzeitig, ob Ihre Produkte vom AI Act betroffen sind, und entwickeln Sie eine klare Umsetzungsstrategie, damit die Marktzulassung nicht ins Stocken gerät.


Cybersecurity und AI Act: Unverzichtbar für KI-basierte IVD
Cybersecurity oder Cybersicherheit ist nicht nur technische Notwendigkeit, sondern regulatorische Pflicht. IVD-Systeme, die mit KI arbeiten, müssen so konzipiert sein, dass sie sicher gegenüber Manipulation, Datenverlust und Fehlfunktionen sind, und das über den gesamten Lebenszyklus hinweg.
Anforderungen an die Sicherheit von KI in IVD-Systemen:
- Schutz der Patientendaten und Eingabedaten
- nachvollziehbare Entscheidungslogik und Audit-Trails
- Protokollierung und Monitoring der Systemaktivitäten
- Frühwarnmechanismen für unerwünschte Effekte
- Sicherheitsstrategie als Teil des Qualitätsmanagementsystems
Das Positionspapier "European Artificial Intelligence Act" von Team-NB vom April 2025 macht deutlich: Cybersicherheit bei KI in Medizinprodukten geht weit über klassische IT Security hinaus. Die Architektur muss regulatorisch nachvollziehbar und technisch belastbar sein, und zwar von Anfang an.Wir zeigen Ihnen, wie Sie Cybersicherheit und Regulatorik klug miteinander verknüpfen, damit Ihr IVD-System auch unter KI-Einsatz zuverlässig zugelassen werden kann.Cybersicherheit im Griff, von Anfang an. Holen Sie sich jetzt gezielte Unterstützung für Ihr KI-IVD. Wir freuen uns, Sie kennenzulernen!
AI Act für IVD: Wer jetzt handelt, bleibt handlungsfähig
Der AI Act ist längst Realität: Die Übergangsfristen haben begonnen, und viele der AI-Act-Vorgaben überschneiden sich mit bestehenden Anforderungen aus der IVDR und internationalen Normen. Für IVD-Hersteller mit KI-Elementen in ihren Produkten ist das ein Weckruf: Wer zu spät reagiert, riskiert Verzögerungen, Ressourcenengpässe und hohe Korrekturkosten.Jetzt ist der richtige Zeitpunkt für eine fundierte Bestandsaufnahme – aus drei guten Gründen:1. Korrekturen kosten, Prävention rechnet sich
Wer erst auf Anforderungen reagiert, wenn Prüfstellen oder Behörden sie einfordern, muss häufig aufwendig nachbessern. Eine frühzeitige Bewertung der KI-Komponenten im Kontext des AI Acts spart Zeit und reduziert Zulassungsrisiken.2. Produktentwicklung braucht regulatorische Klarheit
KI-Features werden oft technisch geplant, bevor regulatorisch bewertet wurde, ob sie unter den AI Act fallen. Frühzeitige Einordnung hilft, spätere Umwege in Entwicklung, Dokumentation und Risikoanalyse zu vermeiden.3. Regulatorische Weitsicht schafft Vertrauen
Unternehmen, die den AI Act aktiv in ihre Entwicklungsstrategie integrieren, zeigen Verantwortung gegenüber Behörden, Marktpartnern und Usern. Das erhöht nicht nur die Chance auf reibungslose Zulassungen, sondern auch auf langfristige Marktakzeptanz.Wir unterstützen Sie dabei, regulatorisch sicher und strategisch zukunftsfähig aufgestellt zu sein.Vereinbaren Sie Ihr Orientierungsgespräch – unverbindlich, aber entscheidend. Wir sind für alle Ihre Fragen bereit.