Materialänderung, Nachhaltigkeit und biologische Sicherheit von Medizinprodukten – Ein Ausflug in den regulatorischen Dschungel
31.05.2024
Sie haben Fragen zum Beitrag oder möchten mehr über unsere Leistungen erfahren? Wir freuen uns auf Ihre Nachricht!Jetzt unverbindlich anfragen
Seit Inkrafttreten der Medizinprodukteverordnung (Medical Device Regulation (EU) 2017/745 (MDR)) im Jahr 2017 hat sich einiges getan. Für manche Unternehmen stellen die MDR-Anforderungen weiterhin Probleme dar, während sich andere schon mit der Umsetzung zahlreicher weiterer Richtlinien und Verordnungen beschäftigen, die sich aufgrund der MDR ergeben haben. Neben diesen Regularien gilt es heutzutage noch weitere Dinge, wie z. B. Nachhaltigkeit, zu beachten. Gerade im Hinblick auf potenzielle oder notwendige Materialänderungen von Medizinprodukten, müssen in der aktuellen Lage neben den gegenwärtigen Anforderungen z.B. zur biologischen Sicherheit auch bereits mehrere Schritte in die Zukunft gedacht werden, um solche Änderungen nachhaltig und wirtschaftlich zu gestalten. Lassen Sie uns gemeinsam einen Ausflug in den Dschungel der Anforderungen wagen.
Der Hauptfokus der MDR liegt auf der Nachweiserbringung zur Sicherheit und Leistung eines Medizinprodukts über dessen gesamten Lebenszyklus. Welche Nachweise gefordert werden, lässt sich in den grundlegenden Sicherheits- und Leistungsanforderungen im Anhang I der MDR nachschauen. In Kapitel II widmet sich der Abschnitt 10.4 komplett dem Thema "Stoffe" und den Fragen, welche Stoffe hierbei erlaubt sind sowie welche besonderer Aufmerksamkeit bedürfen.Generell sollen Medizinprodukte so ausgelegt und hergestellt werden, dass die Risiken durch Stoffe oder Partikel, die aus dem Produkt freigesetzt werden können, einschließlich Abrieb, Abbauprodukten und Verarbeitungsrückständen, so weit wie möglich verringert werden.Wenn es sich um kritischere Medizinprodukte handelt, die< 0,1 % Massenanteil verwendet werden. Sollen solche Stoffe in größeren Maßstäben verwendet werden und ist die direkte, invasive Anwendung vorgesehen, ist für den Einsatz eine Rechtfertigung notwendig, deren Inhalte in den Abschnitten 10.4.2 – 10.4.5 der MDR behandelt werden.Generell muss bei einer solchen Rechtfertigung immer auf die neuesten wissenschaftlichen Erkenntnisse und weitere EU-Verordnungen oder Leitlinien eingegangen werden. Diese werden dann auf das eigene Medizinprodukt übertragen, um produktspezifisch eine fundierte Rechtfertigung und Bewertung zu erhalten. Sind kritische Stoffe in höherem Massenanteil in den Anwendungsteilen des Medizinprodukts enthalten, muss eine Kennzeichnung über das Vorhandensein solcher Stoffe auf den Produkten selbst oder der Einzelverpackung erfolgen. Eine genaue Auflistung der betroffenen Stoffe ist ebenfalls erforderlich. Patientengruppen, die als besonders anfällig für solche Stoffe und/oder Werkstoffe gelten, werden über Restrisiken und eventuelle Vorsichtsmaßnahmen in der Gebrauchsanweisung informiert.
Ist eine Änderung eines Rohmaterials für ein Medizinprodukt vorgesehen, bedeutet das nicht zwangsläufig, dass alle bisher gültigen Tests zum Nachweis der Biokompatibilität nicht mehr anwendbar sind. Vielmehr ist die Bewertung solcher Änderungen vorgelagert im Rahmen des Risikomanagementsystems gemäß ISO 14971 (aktuell EN ISO 14971:2019+A11:2021) vorzunehmen. Dabei müssen die potenziellen Auswirkungen der Änderung betrachtet werden, die je nach vorgesehener Änderung unterschiedliche Ergebnisse liefern können.Werden hierbei nicht vertretbare Risiken identifiziert, sind die Hersteller dazu verpflichtet diese im Rahmen der Anforderungen gemäß ISO 10993-1 (aktuell EN ISO 10993-1:2020) in einer neuen Version des biologischen Bewertungsplans zu benennen. Zusätzlich muss eine wissenschaftliche Literaturrecherche, in Bezug auf das vorgesehene neue Material und die vorgesehene klinische Anwendung des Medizinprodukts, durchgeführt werden, da nur mit einer ausreichenden physikalischen und chemischen Charakterisierung eine fundierte Aussage über die biologische Sicherheit getroffen werden kann. Weiterhin müssen die Endpunkte, die sich ebenfalls aus der EN ISO 10993-1:2020 – Annex A, Tabelle A.1 ergeben, betrachtet und in Bezug auf die vorgesehene Materialänderung bewertet werden. Sollte sich das Risiko im Anschluss immer noch im nicht akzeptablen Bereich befinden oder keine passenden Literaturdaten zu finden sein, dann folgt die Erstellung einer neuen Teststrategie mit der anschließenden finalen Bewertung im Rahmen der Erstellung einer neuen Version des biologischen Bewertungsberichts.
Neben der MDR und den dort genannten weiteren Anforderungen, sollten auch immer neueste Entwicklungen und Beschlüsse innerhalb der EU betrachtet werden, da diese, auch wenn die MDR nicht direkt betroffen ist, durchaus eine Auswirkung auf Medizinprodukte haben können. Dies kann beispielsweise anhand der aktuellen Entwicklungen zur Nachhaltigkeit im Rahmen desEU Green Deal und der diskutierten Beschränkung von per- und polyfluorierten Alkylsubstanzen (PFAS) beobachtet werden.Die Ziele des EU Green Deal benennen die Etablierung einer modernen, ressourceneffizienten und wettbewerbsfähigen Wirtschaft mit dem Ziel bis 2050 keine Netto-Treibhausgase mehr zu emittieren. Auch hier müssen die Medizinprodukteindustrie und die jeweiligen Hersteller Auflagen einhalten. Hierbei besteht die Herausforderung das technisch Mögliche regulatorisch sinnvoll und wirtschaftlich im Unternehmen zu integrieren.Teil des Green Deal ist auch die Überarbeitung der REACH Verordnung (Regulation (EC) No 1907/2006 concerning the Registration, Evaluation, Authorisation and Restriction of Chemicals (REACH)) bzw. generell eine neue Chemikalienstrategie. Diese zielt darauf ab, den Menschen sowie die Umwelt besser vor schädlichen Chemikalien zu schützen und Innovationen durch die Förderung der Verwendung sichererer und nachhaltigerer Chemikalien voranzutreiben. Um dieses Ziel zu erreichen, wurde im Februar 2023 ein Vorschlag zur Beschränkung einer kompletten Stoffgruppe, der PFAS, bei der Europäischen Chemikalienagentur (ECHA) eingereicht.PFAS weisen amphiphile Eigenschaften auf. Das heißt sie haben neben hydrophoben Kohlenstoff-Fluor Verbindungen auch hydrophile Anteile durch die Kopfgruppe. Aufgrund dieser amphiphilen Eigenschaften in Kombination mit der hohen Hitzebeständigkeit sind die Stoffe chemisch sehr inert (träge) und reichern sich so in der Umwelt an und können weitreichende Auswirkungen auf die menschliche Gesundheit haben.Die Herstellung, Inverkehrbringung und Verwendung dieser Stoffgruppe soll nun durch den eingereichten Vorschlag sukzessive beschränkt werden. Dabei sieht der Verbotsvorschlag für Medizinprodukte eine Übergangsregelung von 13,5 Jahren vor (18 Monate plus 12 Jahre Ausnahmeregelung). Bis September 2023 konnten im Rahmen eines Konsultationsverfahren Kommentare zu dem eingereichten Verbotsentwurf eingereicht werden, die von Fachausschüssen der ECHA gesichtet werden. Mit einer Stellungnahme der ECHA wird im Jahr 2024 gerechnet, wobei sich bisher nur erahnen lässt welche Änderungen eingebracht werden. Dennoch ist absehbar, dass die gesamte Stoffgruppe der PFAS beschränkt und es lediglich für notwendige Bereiche, wie u.a. die Medizintechnikindustrie, Ausnahmen geben wird. Deshalb ist die Aufgabe der Medizinproduktehersteller nun klar – sich auf das bevorstehende Verbot bestmöglich vorzubereiten.Unabhängig davon, ob es um den zukünftigen Einsatz der PFAS oder nachhaltigerer Kunststoffe wie biobasierten oder recyclierten Kunststoffen im Medizinprodukt geht, ist die gezielte Etablierung einer sinnvollen Datenlage immer vonnöten.Im Folgenden werden die verschiedenen Möglichkeiten aufgezeigt, wie zukünftig biobasierte bzw. recyclierte Kunststoffe in Medizinprodukten verwendet oder PFAS-haltige Medizinprodukte vorerst sicher auf den Markt gebracht werden können.
Um der bevorstehenden Beschränkung der PFAS strategisch entgegen treten zu können, ist eine Auflistung des Produktportfolios inklusive der verwendeten Materialien unabdingbar. Werden hierbei essenzielle PFAS identifiziert, gilt es direkt zu handeln. Der erste Schritt ist immer die frühzeitige Kommunikation mit allen Stakeholdern, um sicherzustellen, dass z. B. Zulieferer auch weiterhin Rohstoffe liefern und nicht aufgrund der Beschränkung alle PFAS-Komponente abkündigen. Der Ursprung der vollumfassenden PFAS-Beschränkung liegt neben den kritischen Eigenschaften auch in der häufig fehlenden Datenlage im Hinblick auf die Auswirkungen der PFAS auf die Umwelt und Gesundheit, weshalb es wichtig sein wird, für Medizinprodukte eine durchdachte sowie maßgeschneiderte Bewertungsstrategie aufzusetzen, um alle potenziellen Risiken adäquat mindern zu können. Diese kann wie folgt aussehen:
 Abbildung 1: Mögliche Bewertungsstrategie für Medizinprodukte; Abkürzungen: CMR = cancerogenic, mutagenic, toxic to reproduction, ED = endokrin disruptiv
Abbildung 1: Mögliche Bewertungsstrategie für Medizinprodukte; Abkürzungen: CMR = cancerogenic, mutagenic, toxic to reproduction, ED = endokrin disruptiv
Die vorgestellte Strategie bietet nun die Möglichkeit, eine datenbasierte Bewertung von Medizinprodukten in Bezug auf deren klinischen Gebrauch durchzuführen. So kann ein Nachweis geliefert werden, dass der Gebrauch der Medizinprodukte trotz PFAS-Einsatz keine biologischen und toxikologischen Risiken birgt. Zusätzlich können in der Gebrauchsanweisung weitere Warn- und Entsorgungshinweise ergänzt werden, die die unkontrollierte Freisetzung einschränken, welche derzeit das Hauptproblem darstellt, und so ggf. eine Kreislaufwirtschaft oder zumindest eine kontrollierte Entsorgung der Medizinprodukte ermöglichen.Durch diese Strategie kann vorerst sichergestellt werden, dass die Sicherheit und Wirksamkeit bereits auf dem Markt befindlicher PFAS-haltiger Medizinprodukte gewährleistet sind. Langfristig ist es jedoch von entscheidender Bedeutung, dass der Einsatz von PFAS reduziert wird, und dass durch Forschung und Entwicklung Substitute für PFAS entwickelt werden, die in innovativen Medizinprodukten, aber auch bei bereits auf dem Markt befindlichen Produkten, berücksichtigt werden.Darüber hinaus gibt es noch weitere Möglichkeiten für Hersteller, sich auf ein bevorstehendes PFAS-Verbot vorzubereiten:
Ein Ziel des EU Green Deal ist die Reduktion der Netto-Treibhausgasemissionen bis zur kompletten Klimaneutralität im Jahr 2050. Aber auch die Abkopplung des Wachstums von der Ressourcennutzung und niemanden, weder Mensch noch Region, im Stich zu lassen, stehen im Fokus, um den Übergang zu einer modernen, ressourceneffizienten und wettbewerbsfähigen Wirtschaft zu schaffen. Dabei ist der EU Green Deal eng mit dem Begriff "Nachhaltigkeit" verbunden. Die Dimensionen der Nachhaltigkeit umfassen neben der ökologischen auch die soziale und die wirtschaftliche Nachhaltigkeit. Diese beeinflussen sich gegenseitig und müssen gleichermaßen berücksichtigt werden.Doch wie kann der vielumfassende Begriff "Nachhaltigkeit" für die Medizinprodukteindustrie eingegrenzt werden? Ein denkbarer Ansatz, um den Inhalten des Green Deal Folge zu leisten, ist der Einsatz nachhaltiger Ressourcen. Dies sind z. B.
Allein diese beiden Beispiele verdeutlichen, dass die erforderliche Nachweislage sich in Zukunft nicht verringern wird. Auch im Hinblick auf die verschiedenen Regularien bleibt der Kampf durch einen Urwald von Anforderungen nicht aus, der im Folgenden etwas übersichtlicher dargestellt wird:
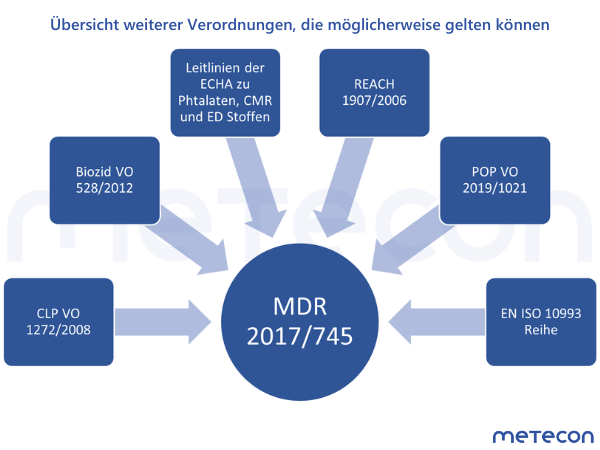
Abbildung 2: Übersicht weiterer Verordnungen, die zusätzlich gelten können. Abkürzungen: MDR = Medical Device Regulation; CLP VO = Verordnung zur Einstufung, Kennzeichnung und Verpackung von Stoffen und Gemischen (CLP: Classification, Labeling, Packaging); ECHA = European Chemical Agency; REACH = Verordnung zur Registrierung, Bewertung, Zulassung und Beschränkung chemischer Stoffe (REACH: Registration, Evaluation, Authorisation and Restriction of Chemicals); POP VO = Verordnung über persistente organische Schadstoffe (POP = persistent organic pollutants); EN = europäische Norm; ISO = International Organization for StandardizationIm Falle der Medizinprodukte bleibt die MDR als Leitverordnung bestehen, weshalb sich an den Nachweisen zur biologischen Sicherheit gemäß den normativen Angaben der EN ISO 10993-Reihe primär nichts ändert. Dennoch wird auf weitere Verordnungen oder Veröffentlichungen wie die der ECHA verwiesen. Diese Anforderungen gilt es zu berücksichtigen und sicherzustellen, dass die Lieferanten ihren Aufgaben im Rahmen von z. B. REACH nachkommen. Ebenfalls ergeben sich immer wieder Neuerungen und Ergänzungen der zusätzlichen Verordnungen, die Auswirkungen auf die Medizinprodukte mit sich bringen können, weshalb eine Auseinandersetzung mit den Verordnungen erfolgen muss.
Die Zukunft der Medizinprodukte und die Anforderungen an die biologische Sicherheit werden sicherlich spannend bleiben, gerade im Hinblick auf potenzielle Verbote unter REACH, die vermutlich eher zu- als abnehmen werden. Nach Einführung der MDR im Jahr 2017 blieb zu Beginn der Aktionismus der Unternehmen aus, was zu Verzögerungen im Rahmen der Zertifizierungen geführt hat. Aus diesen Fehlern sollte nun gelernt werden, auch wenn es zunächst als großer, kostspieliger Aufwand erscheint. Deshalb sollten Hersteller nun ins Handeln kommen:
Dieser Beitrag ist im Auftrag der BIOPRO Baden-Württemberg GmbH entstanden. Die Landesgesellschaft BIOPRO Baden-Württemberg unterstützt mit ihren Kompetenzen die Transformation von Wirtschaft und Gesellschaft mit Fokus auf die Gesundheitsindustrie mit ihren Branchen Biotechnologie, Medizintechnik und Pharmazeutischer Industrie in Baden-Württemberg. Als Innovationsagentur setzt sie Impulse für die Entwicklung der Gesundheitsindustrie, initiiert Kooperationen, begleitet Innovationen sowie Gründungen und unterstützt die nachhaltige Transformation von gesundheitswirtschaftsbezogenen Liefer- und Nutzungsketten. Als Anlaufstelle Regulatorik Gesundheitswirtschaft BW, gefördert durch das Ministerium für Wirtschaft, Arbeit und Tourismus Baden-Württemberg, unterstützt die BIOPRO die baden-württembergischen Unternehmen der Gesundheitsindustrie bei der Umsetzung neuer regulatorischer Anforderungen. Weitere Informationen über die Aktivitäten als Anlaufstelle Regulatorik Gesundheitswirtschaft: https://regulatorik-gesundheitswirtschaft.bio-pro.de
 Dr. Carolin Schilpp
Dr. Carolin Schilpp
Anforderungen der MDR an Werkstoffe und Stoffe
Der Hauptfokus der MDR liegt auf der Nachweiserbringung zur Sicherheit und Leistung eines Medizinprodukts über dessen gesamten Lebenszyklus. Welche Nachweise gefordert werden, lässt sich in den grundlegenden Sicherheits- und Leistungsanforderungen im Anhang I der MDR nachschauen. In Kapitel II widmet sich der Abschnitt 10.4 komplett dem Thema "Stoffe" und den Fragen, welche Stoffe hierbei erlaubt sind sowie welche besonderer Aufmerksamkeit bedürfen.Generell sollen Medizinprodukte so ausgelegt und hergestellt werden, dass die Risiken durch Stoffe oder Partikel, die aus dem Produkt freigesetzt werden können, einschließlich Abrieb, Abbauprodukten und Verarbeitungsrückständen, so weit wie möglich verringert werden.Wenn es sich um kritischere Medizinprodukte handelt, die
- invasiv angewandt werden und direkten Körperkontakt haben
- dem Körper Arzneimittel, Körperflüssigkeiten oder sonstige Stoffe, einschließlich Gase, (wiederholt) verabreichen oder entnehmen, oder
- solche Arzneimittel, Körperflüssigkeiten oder sonstige Stoffe, einschließlich Gase, die dem Körper (wiederholt) verabreicht werden, transportieren oder lagern
- kanzerogenen (krebserregenden, carcinogenic),
- mutagenen (Veränderung das Erbgut, mutagenic)
- oder reproduktionstoxischen Eigenschaften (Beeinträchtigung der Fruchtbarkeit bei Frau und Mann und/oder Entwicklung der Nachkommen, toxic to reproduction)
- und Stoffe mit endokrin wirkenden Eigenschaften (ED = endokrin disruptiv, endocrine disruptors), also mit Auswirkungen auf das Hormonsystem,
Einfluss einer (Roh-)Materialänderung auf die biologische Sicherheit
Ist eine Änderung eines Rohmaterials für ein Medizinprodukt vorgesehen, bedeutet das nicht zwangsläufig, dass alle bisher gültigen Tests zum Nachweis der Biokompatibilität nicht mehr anwendbar sind. Vielmehr ist die Bewertung solcher Änderungen vorgelagert im Rahmen des Risikomanagementsystems gemäß ISO 14971 (aktuell EN ISO 14971:2019+A11:2021) vorzunehmen. Dabei müssen die potenziellen Auswirkungen der Änderung betrachtet werden, die je nach vorgesehener Änderung unterschiedliche Ergebnisse liefern können.Werden hierbei nicht vertretbare Risiken identifiziert, sind die Hersteller dazu verpflichtet diese im Rahmen der Anforderungen gemäß ISO 10993-1 (aktuell EN ISO 10993-1:2020) in einer neuen Version des biologischen Bewertungsplans zu benennen. Zusätzlich muss eine wissenschaftliche Literaturrecherche, in Bezug auf das vorgesehene neue Material und die vorgesehene klinische Anwendung des Medizinprodukts, durchgeführt werden, da nur mit einer ausreichenden physikalischen und chemischen Charakterisierung eine fundierte Aussage über die biologische Sicherheit getroffen werden kann. Weiterhin müssen die Endpunkte, die sich ebenfalls aus der EN ISO 10993-1:2020 – Annex A, Tabelle A.1 ergeben, betrachtet und in Bezug auf die vorgesehene Materialänderung bewertet werden. Sollte sich das Risiko im Anschluss immer noch im nicht akzeptablen Bereich befinden oder keine passenden Literaturdaten zu finden sein, dann folgt die Erstellung einer neuen Teststrategie mit der anschließenden finalen Bewertung im Rahmen der Erstellung einer neuen Version des biologischen Bewertungsberichts.
PFAS und nachhaltige Kunststoffe – aktuelle Möglichkeiten zum Einsatz
Neben der MDR und den dort genannten weiteren Anforderungen, sollten auch immer neueste Entwicklungen und Beschlüsse innerhalb der EU betrachtet werden, da diese, auch wenn die MDR nicht direkt betroffen ist, durchaus eine Auswirkung auf Medizinprodukte haben können. Dies kann beispielsweise anhand der aktuellen Entwicklungen zur Nachhaltigkeit im Rahmen des
Per- und polyfluorierte Alkylsubstanzen – PFAS
Um der bevorstehenden Beschränkung der PFAS strategisch entgegen treten zu können, ist eine Auflistung des Produktportfolios inklusive der verwendeten Materialien unabdingbar. Werden hierbei essenzielle PFAS identifiziert, gilt es direkt zu handeln. Der erste Schritt ist immer die frühzeitige Kommunikation mit allen Stakeholdern, um sicherzustellen, dass z. B. Zulieferer auch weiterhin Rohstoffe liefern und nicht aufgrund der Beschränkung alle PFAS-Komponente abkündigen. Der Ursprung der vollumfassenden PFAS-Beschränkung liegt neben den kritischen Eigenschaften auch in der häufig fehlenden Datenlage im Hinblick auf die Auswirkungen der PFAS auf die Umwelt und Gesundheit, weshalb es wichtig sein wird, für Medizinprodukte eine durchdachte sowie maßgeschneiderte Bewertungsstrategie aufzusetzen, um alle potenziellen Risiken adäquat mindern zu können. Diese kann wie folgt aussehen:
 Abbildung 1: Mögliche Bewertungsstrategie für Medizinprodukte; Abkürzungen: CMR = cancerogenic, mutagenic, toxic to reproduction, ED = endokrin disruptiv
Abbildung 1: Mögliche Bewertungsstrategie für Medizinprodukte; Abkürzungen: CMR = cancerogenic, mutagenic, toxic to reproduction, ED = endokrin disruptivDie vorgestellte Strategie bietet nun die Möglichkeit, eine datenbasierte Bewertung von Medizinprodukten in Bezug auf deren klinischen Gebrauch durchzuführen. So kann ein Nachweis geliefert werden, dass der Gebrauch der Medizinprodukte trotz PFAS-Einsatz keine biologischen und toxikologischen Risiken birgt. Zusätzlich können in der Gebrauchsanweisung weitere Warn- und Entsorgungshinweise ergänzt werden, die die unkontrollierte Freisetzung einschränken, welche derzeit das Hauptproblem darstellt, und so ggf. eine Kreislaufwirtschaft oder zumindest eine kontrollierte Entsorgung der Medizinprodukte ermöglichen.Durch diese Strategie kann vorerst sichergestellt werden, dass die Sicherheit und Wirksamkeit bereits auf dem Markt befindlicher PFAS-haltiger Medizinprodukte gewährleistet sind. Langfristig ist es jedoch von entscheidender Bedeutung, dass der Einsatz von PFAS reduziert wird, und dass durch Forschung und Entwicklung Substitute für PFAS entwickelt werden, die in innovativen Medizinprodukten, aber auch bei bereits auf dem Markt befindlichen Produkten, berücksichtigt werden.Darüber hinaus gibt es noch weitere Möglichkeiten für Hersteller, sich auf ein bevorstehendes PFAS-Verbot vorzubereiten:
- Modulierung der PFAS, um z. B. einen schnelleren, toxikologisch unbedenklichen Abbau zu ermöglichen
- Modulierung der Medizinprodukte, um eine potenzielle Freisetzung der PFAS einzuschränken
- Hersteller und Lieferanten können eine medizinische Ausnahme der nötigen Stoffe beantragen (aufwendig).
- Registrierung und Zulassung der Stoffe bei der zuständigen Behörde als Interessenverband mehrerer Hersteller und Lieferanten/Zulieferer
Nachhaltigere Kunststoffe in Medizinprodukten
Ein Ziel des EU Green Deal ist die Reduktion der Netto-Treibhausgasemissionen bis zur kompletten Klimaneutralität im Jahr 2050. Aber auch die Abkopplung des Wachstums von der Ressourcennutzung und niemanden, weder Mensch noch Region, im Stich zu lassen, stehen im Fokus, um den Übergang zu einer modernen, ressourceneffizienten und wettbewerbsfähigen Wirtschaft zu schaffen. Dabei ist der EU Green Deal eng mit dem Begriff "Nachhaltigkeit" verbunden. Die Dimensionen der Nachhaltigkeit umfassen neben der ökologischen auch die soziale und die wirtschaftliche Nachhaltigkeit. Diese beeinflussen sich gegenseitig und müssen gleichermaßen berücksichtigt werden.Doch wie kann der vielumfassende Begriff "Nachhaltigkeit" für die Medizinprodukteindustrie eingegrenzt werden? Ein denkbarer Ansatz, um den Inhalten des Green Deal Folge zu leisten, ist der Einsatz nachhaltiger Ressourcen. Dies sind z. B.
- Recycelte Kunststoffe: Diese bestehen aus wiederaufbereiteten Kunststoffabfällen, die meist in einem chemischen oder mechanischen Recyclingprozess gewonnen werden. Bei recycelten Kunststoffen wird zwischen Post-Consumer-Rezyklaten – recyceltem Kunststoff aus Haushaltsabfällen – und Post-Industrial-Rezyklaten – recyceltem Kunststoff aus "Abfällen" anderer Industrien wie z.B. Speiseölraffinerien – unterschieden.
- Biobasierte Kunststoffe: Dabei handelt es sich um Kunststoffe aus nachwachsenden Rohstoffen.
- Biologisch abbaubare Kunststoffe: Zu den biologisch abbaubaren Kunststoffen zählen all jene Kunststoffe, die durch Mikroorganismen zersetzt werden können.
- Die Verwendung von rein biobasierten Kunststoffen ist heute noch nicht gängig, aber erste Ansätze finden bereits ihren Weg in die Praxis. Dennoch werden aktuell meist Mischungen aus fossilen und biobasierten Kunststoffen in unterschiedlichen Anteilen verwendet. Grund für die Mischung ist, dass meist nur so die gewünschten Eigenschaften wie Stabilität, Reinheit sowie thermische und mechanische Belastbarkeit erreicht werden können. Es gibt aber auch Polymere wie Polyethylen, Polymilchsäuren (Polylactide), Polyhydroxyalkanoate (PAH), Polybutylensuccinat (PBS) oder Poly (hydroxybutyrat-co-hydroxyvalerat)-Copolymere (PHBV), die 100 % biobasiert eingesetzt werden können.
- Während die Verwendung von Kunststoffen mit Rezyklat-Anteil beispielsweise bereits bei Verpackungen von Medizinprodukten fallweise möglich ist, ist der Einsatz von Rezyklaten für höher klassifizierte Medizinprodukte ohne Standardisierung in der Herstellung von Rezyklaten durch z.B. gleichbleibende Qualität und immer gleichen Rezyklat-Anteil momentan nahezu unmöglich.
Anforderungen an die Nachweislage – was ist notwendig?
Allein diese beiden Beispiele verdeutlichen, dass die erforderliche Nachweislage sich in Zukunft nicht verringern wird. Auch im Hinblick auf die verschiedenen Regularien bleibt der Kampf durch einen Urwald von Anforderungen nicht aus, der im Folgenden etwas übersichtlicher dargestellt wird:

Abbildung 2: Übersicht weiterer Verordnungen, die zusätzlich gelten können. Abkürzungen: MDR = Medical Device Regulation; CLP VO = Verordnung zur Einstufung, Kennzeichnung und Verpackung von Stoffen und Gemischen (CLP: Classification, Labeling, Packaging); ECHA = European Chemical Agency; REACH = Verordnung zur Registrierung, Bewertung, Zulassung und Beschränkung chemischer Stoffe (REACH: Registration, Evaluation, Authorisation and Restriction of Chemicals); POP VO = Verordnung über persistente organische Schadstoffe (POP = persistent organic pollutants); EN = europäische Norm; ISO = International Organization for StandardizationIm Falle der Medizinprodukte bleibt die MDR als Leitverordnung bestehen, weshalb sich an den Nachweisen zur biologischen Sicherheit gemäß den normativen Angaben der EN ISO 10993-Reihe primär nichts ändert. Dennoch wird auf weitere Verordnungen oder Veröffentlichungen wie die der ECHA verwiesen. Diese Anforderungen gilt es zu berücksichtigen und sicherzustellen, dass die Lieferanten ihren Aufgaben im Rahmen von z. B. REACH nachkommen. Ebenfalls ergeben sich immer wieder Neuerungen und Ergänzungen der zusätzlichen Verordnungen, die Auswirkungen auf die Medizinprodukte mit sich bringen können, weshalb eine Auseinandersetzung mit den Verordnungen erfolgen muss.
Fazit
Die Zukunft der Medizinprodukte und die Anforderungen an die biologische Sicherheit werden sicherlich spannend bleiben, gerade im Hinblick auf potenzielle Verbote unter REACH, die vermutlich eher zu- als abnehmen werden. Nach Einführung der MDR im Jahr 2017 blieb zu Beginn der Aktionismus der Unternehmen aus, was zu Verzögerungen im Rahmen der Zertifizierungen geführt hat. Aus diesen Fehlern sollte nun gelernt werden, auch wenn es zunächst als großer, kostspieliger Aufwand erscheint. Deshalb sollten Hersteller nun ins Handeln kommen:
- Überblick über Rohstoffe verschaffen
- Auflisten aller potenziell betroffenen Rohstoffe/Medizinprodukte, welche von Änderungen durch Verbote nach REACH wie z. B. dem PFAS-Verbot betroffen wären oder bei denen der Einsatz nachhaltiger Werkstoffe angestrebt wird
- Priorisierung nach der Wichtigkeit bzw. Notwendigkeit der Medizinprodukte: Wenn beispielsweise durch das Verbot von PFAS behandelbare Krankheiten nicht mehr behandelt werden können, dann haben solche Produkte Vorrang.
- Priorisierung gemäß Notwendigkeit des Einsatzes der verbotenen Stoffe/Materialien und Notwendigkeit der Änderung
- Argumentationsgrundlage durch umfangreiche Risikoanalyse und Charakterisierung der vorgesehenen Stoffe und Medizinprodukte schaffen
- „Verbündete“ suchen für Interessenverband und Beantragung medizinischer Ausnahmen
- Nachhaltigkeit kann auf vielen Ebenen stattfinden und muss nicht immer direkt am kritischsten Punkt, wie z. B. einer kompletten Materialänderung ansetzen: Die Materialreduktion der fossilen Rohstoffe im Produkt selbst wäre ein denkbarer Ansatz.
- Biobasierte oder recyclierte Kunststoffe für den Einsatz in Medizinprodukten für Komponenten ohne direkten Körperkontakt als ersten Schritt nutzen, da sonst schwer ein sinnvolles Kosten-Nutzen Verhältnis zu erreichen ist. Dieser Punkt sollte auch bei der Entwicklung neuer Produkte bereits von vorneherein mitgedacht werden.
Dieser Beitrag ist im Auftrag der BIOPRO Baden-Württemberg GmbH entstanden. Die Landesgesellschaft BIOPRO Baden-Württemberg unterstützt mit ihren Kompetenzen die Transformation von Wirtschaft und Gesellschaft mit Fokus auf die Gesundheitsindustrie mit ihren Branchen Biotechnologie, Medizintechnik und Pharmazeutischer Industrie in Baden-Württemberg. Als Innovationsagentur setzt sie Impulse für die Entwicklung der Gesundheitsindustrie, initiiert Kooperationen, begleitet Innovationen sowie Gründungen und unterstützt die nachhaltige Transformation von gesundheitswirtschaftsbezogenen Liefer- und Nutzungsketten. Als Anlaufstelle Regulatorik Gesundheitswirtschaft BW, gefördert durch das Ministerium für Wirtschaft, Arbeit und Tourismus Baden-Württemberg, unterstützt die BIOPRO die baden-württembergischen Unternehmen der Gesundheitsindustrie bei der Umsetzung neuer regulatorischer Anforderungen. Weitere Informationen über die Aktivitäten als Anlaufstelle Regulatorik Gesundheitswirtschaft: https://regulatorik-gesundheitswirtschaft.bio-pro.de
Unsere Blogbeiträge werden mit höchster Sorgfalt recherchiert und erstellt, sind jedoch lediglich Momentaufnahmen in der Regulatorik, und diese ist in stetem Wandel. Wir gewährleisten nicht, dass ältere Inhalte noch aktuell und aussagekräftig sind. Wenn Sie nicht sicher sind, ob der Beitrag, den Sie auf dieser Seite gelesen haben, noch dem aktuellen Stand der Regulierung entspricht, nehmen Sie bitte Kontakt zu uns auf: Wir ordnen Ihr Thema schnell in den aktuellen Kontext ein.

Team Lead Biological Safety
Regulatory Affairs & Technical Documentation


