Change-Management im Qualitätsmanagement: Die 5 Phasen erfolgreicher Veränderungen in der Medizintechnik
27.05.2025
Sie haben Fragen zum Beitrag oder möchten mehr über unsere Leistungen erfahren? Wir freuen uns auf Ihre Nachricht!Jetzt unverbindlich anfragen
Veränderungen sind in der Medizintechnik unvermeidlich: ob durch neue regulatorische Anforderungen, digitale Transformation oder strategische Neuausrichtungen. Sei es die Einführung eines RIM-Systems (Regulatory Information Management System) oder eines elektronischen Qualitätsmanagement-Systems (eQMS) - erfolgreiches Change-Management bedeutet mehr als nur die Anpassung von Prozessen und Strukturen. Entscheidend ist, wie gut die Menschen im Unternehmen in den Veränderungsprozess eingebunden werden.In unserem Beitrag Change-Management im Qualitätsmanagement – Erfolgreicher Wandel in der Medizintechnik haben wir die zentralen Herausforderungen und Erfolgsfaktoren im Change-Management beleuchtet. Wir haben uns angesehen, warum Akzeptanz, Kommunikation und Unternehmenskultur eine ebenso große Rolle spielen wie eine klare Strategie und strukturierte Prozesse. Nun geht es darum, die Veränderung gezielt zu gestalten mit einem klaren, praxiserprobten Fünf-Phasen-Modell.Ob Sie nun ein RIM-System oder elektronisches QMS einführen oder eine umfassende Transformation vor sich haben: Mit einem strukturierten Vorgehen lassen sich Veränderungen nicht nur effizient umsetzen, sondern auch nachhaltig verankern.
Phase 1 – Idee
Phase 2 – Planung
Phase 3 – Durchführung
Phase 4 – Überprüfung und Korrektur
 Laura Beer
Laura Beer
Gestaltung einer Veränderung
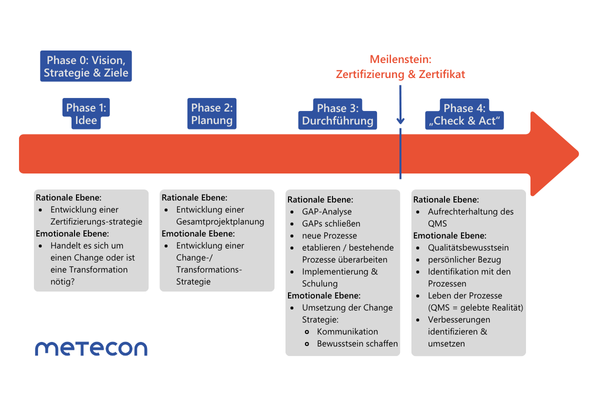
Ein strukturierter Veränderungsprozess lässt sich in fünf Phasen unterteilen:Phase 0 – Vision und StrategiePhase 1 – Idee
Phase 2 – Planung
Phase 3 – Durchführung
Phase 4 – Überprüfung und Korrektur

Phase 0: Vision, Strategie und Ziele
In dieser Phase wird eine klare Vision entwickelt, aus der eine Strategie mit konkreten Zielen abgeleitet wird:- Wo wollen wir hin?
- Was wollen wir?
- Wie können wir das umsetzen?
- Unternehmen 1 (U1): "Wir möchten mit unserem Medizinprodukt erfolgreich im europäischen Markt bestehen."
- Unternehmen 2 (U2): "Unser Unternehmen unterhält ein QMS nach ISO 9001. Um neue Märkte zu erschließen, führen wir die ISO 13485 ein und arbeiten MDR-konform. Wir möchten unsere Produkte nicht nur an Medizinproduktehersteller liefern, sondern selbst Medizinprodukte herstellen und vertreiben."
- U1: Eine Umstellung des QMS von ISO 13485 und MDD auf ISO 13485 und MDR.
- U2: Eine Umstellung des QMS von ISO 9001 auf ISO 13485 & MDR.
Phase 1: Idee
Die Art der Veränderung hängt maßgeblich von der Ausgangslage des Unternehmens ab:- U1: Das Unternehmen ist bereits Medizinproduktehersteller mit einem funktionierenden und zertifizierten QMS. Die Werte und Kultur sind auf die Vision ausgerichtet, sodass nur punktuelle Änderungen und operative Anpassungen notwendig sind. Man spricht in diesem Fall von einem Change-Prozess.
- U2: Das Unternehmen ist derzeit Lieferant für Medizinproduktehersteller; selbst tritt es aber noch nicht als Hersteller von Medizinprodukten auf. Die Umstellung auf ISO 13485 und MDR erfordert ein tiefgreifendes strukturelles Umdenken. Es sind sowohl strukturelle und organisatorische als auch kulturelle Anpassungen notwendig. Man spricht in diesem Fall von einem Transformationsprozess.
Phase 2: Planung
In dieser Phase erfolgt die detaillierte Planung des gesamten Projekts einschließlich der Entwicklung einer Change- bzw. Transformationsstrategie. Bei der Ausgestaltung sind folgende Elemente zu berücksichtigen:Stakeholder Analyse:- Wer ist von der Veränderung betroffen?
- Wer hat direkt oder indirekt Einfluss auf den Projekterfolg?
- Wie unterscheiden sich Risikoaffinität, Stabilitätsbedürfnis und Flexibilität der Beteiligten?
- Welche Veränderungen ergeben sich konkret für die Stakeholder, und wie werden sie voraussichtlich darauf reagieren?
- Welche Kommunikationsbedürfnisse haben die Mitarbeitenden?
- Welche Kanäle und Frequenzen sind für eine wirksame Kommunikation erforderlich?
- Wie werden Kritik & Widerstände identifiziert und ernst genommen?
- Welche Konfliktlösungsstrategien sind vorhanden, welche müssen noch entwickelt werden?
- Wie kann das Bewusstsein für neue Qualitätsstandards gestärkt werden?
- Wie lassen sich Potenziale und persönliche Entwicklungsmöglichkeiten aufzeigen?
- Welche Schulungen und Weiterbildungsmaßnahmen sind notwendig?
Phase 3: Durchführung
Die Umsetzung der geplanten Maßnahmen erfordert eine ganzheitliche Betrachtung der beiden Verändderungsebenen:Rationale Ebene (Projektmanagement):- Durchführung einer GAP-Analyse zur Identifikation von Abweichungen zwischen Ist- und Soll-Zustand
- Festlegung von Maßnahmen zur Schließung der identifizierten Lücken durch Überarbeitung oder Einführung neuer Prozesse
- Einhaltung von Zeitplan und Budget sowie regelmäßiges Reporting
- Frühzeitige Kommunikation des Projekts sowie von Sinn und Zweck der Veränderung
- Offener Umgang mit Ängsten und Unsicherheiten
- Wahrnehmung und aktives Managen von Widerständen
Phase 4: Überprüfung und Korrektur
In der finalen Phase wird überprüft, ob die umgesetzten Maßnahmen den gewünschten Erfolg haben und nachhaltig wirken. Wichtig hierbei ist nach dem Prinzip des PLAN-DO-CHECK-ACT eine aktive Überprüfung der Tauglichkeit sowie der Compliance der neuen bzw. überarbeiteten Prozesse:Tauglichkeitsprüfung- Ist der neue Prozess effektiv und effizient umsetzbar?
- Erreichen wir die gewünschten Ergebnisse?
- Welche KPIs helfen bei der Erfolgsmessung?
- Erfüllen die neuen Prozesse die regulatorischen Anforderungen?
- Überprüfung durch interne Systemaudits mit unabhängigen Auditoren
- Mitarbeitergespräche und aktives Zuhören zur Bewertung der Akzeptanz des überarbeiteten QMS, der angepassten Prozesse und der neuen Kultur
- Förderung einer kontinuierlichen Verbesserung durch offene Rückmeldungen
Und jetzt? So setzen Sie Ihre Pläne in die Tat um
Erfolgreiche Veränderungen folgen einem klaren Prozess, ganz gleich ob es um die Einführung eines RIM-Systems oder eines elektronischen QMS, die Anpassung Ihres Qualitätsmanagements an neue regulatorische Anforderungen oder eine umfassende Transformation geht.Mit einer strukturierten Herangehensweise in fünf Phasen - von der strategischen Vision bis zur nachhaltigen Verankerung - lassen sich Change-Prozesse gezielt steuern und langfristig erfolgreich umsetzen. Entscheidend ist dabei die Kombination aus methodischer Planung, klarer Führung und der aktiven Einbindung aller Beteiligten.Wir unterstützen Sie mit maßgeschneiderten Lösungen: von der Entwicklung einer effizienten Zertifizierungs- und Projektstrategie über Change-Management und Stakeholder-Einbindung bis hin zur Implementierung, Optimierung und Validierung von Systemen und Prozessen.Jede Veränderung bringt Herausforderungen – aber auch enorme Chancen. Lassen Sie uns gemeinsam die beste Strategie für Ihr Unternehmen entwickeln. Vereinbaren Sie jetzt eine unverbindliche Erstberatung und legen Sie den Grundstein für eine erfolgreiche Umsetzung.Jetzt Termin vereinbaren!
Unsere Blogbeiträge werden mit höchster Sorgfalt recherchiert und erstellt, sind jedoch lediglich Momentaufnahmen in der Regulatorik, und diese ist in stetem Wandel. Wir gewährleisten nicht, dass ältere Inhalte noch aktuell und aussagekräftig sind. Wenn Sie nicht sicher sind, ob der Beitrag, den Sie auf dieser Seite gelesen haben, noch dem aktuellen Stand der Regulierung entspricht, nehmen Sie bitte Kontakt zu uns auf: Wir ordnen Ihr Thema schnell in den aktuellen Kontext ein.

Quality Management & Technical Documentation


